La sanitización, desinfección y esterilización de envases plásticos es uno de esos temas donde la confusión terminológica tiene consecuencias nefastas en el proceso de producción. Consecuencias que incluyen riesgos microbiológicos, rechazos de auditoría o incumplimiento normativo.
En una línea de llenado aséptico, ya sea en una planta farmacéutica o en una envasadora de productos cosméticos, el envase es el último punto de contacto antes del producto final, y su tratamiento higiénico no admite ambigüedades. Por ello, en este artículo repasamos los desafíos técnicos que plantea el plástico como material y las herramientas disponibles para diseñar protocolos que funcionen en condiciones reales de producción.
¿Cuál es la diferencia entre sanitizar, desinfectar y esterilizar?
Estos tres términos se usan a veces como sinónimos, pero no lo son. Tienen alcances microbiológicos distintos, y esas diferencias entre sanitizar, desinfectar y esterilizar determinan qué tipo de proceso corresponde según el riesgo sanitario de cada aplicación. Conocerlos con precisión es el punto de partida para cualquier protocolo serio en la industria del plástico.
Sanitización
La sanitización reduce la carga microbiana de una superficie a niveles considerados seguros según criterios regulatorios. Según la Agencia de Protección Ambiental de los Estados Unidos, un sanitizante debe lograr una reducción mínima del 99,9% de bacterias específicas en superficies de contacto con alimentos. No elimina virus ni esporas bacterianas, y no equivale a desinfección.
Es el proceso habitual en superficies de bajo riesgo o en etapas previas al envasado donde la carga inicial es controlada. Su ventaja operativa es la compatibilidad con tiempos de ciclo más cortos y mayor tolerancia de los materiales al agente químico utilizado.
Desinfección
La desinfección apunta a eliminar los microorganismos patógenos presentes en una superficie, incluyendo bacterias, virus y hongos, con una eficiencia que va del 99,99% al 99,999% de reducción. A diferencia de la sanitización, actúa sobre un espectro más amplio de agentes biológicos, aunque no garantiza la eliminación de esporas bacterianas en todos los casos.
Esterilización
La esterilización es un proceso validado que elimina la totalidad de los microorganismos viables de un producto, incluidas esporas bacterianas. El objetivo es alcanzar un nivel de esterilidad que, por ejemplo, en la industria farmacéutica, se expresa como SAL (Sterility Assurance Level) de 10⁻⁶, es decir, una probabilidad menor a 1 en un millón de encontrar una unidad contaminada tras el proceso.
Entre las tecnologías utilizadas para reducción microbiológica avanzada y esterilización de envases se encuentran el vapor de peróxido de hidrógeno, el óxido de etileno y, en determinadas aplicaciones, sistemas complementarios basados en radiación UV-C, cada uno con condicionantes específicos según el tipo de polímero y las características del proceso de llenado.
¿Cuáles son los desafíos en la desinfección de envases plásticos?
Trabajar con plásticos implica un conjunto de restricciones que no aparecen cuando el sustrato es acero inoxidable o vidrio. El material, la geometría del envase y el historial de uso condicionan directamente la eficacia de cualquier agente desinfectante. Veamos cuáles son esos retos:
Compatibilidad de materiales
No todos los desinfectantes son compatibles con todos los plásticos.
- El PET, que domina el mercado de envases de bebidas y alimentos, presenta buena resistencia a soluciones acuosas de peróxido de hidrógeno diluido, pero puede verse afectado por agentes altamente oxidantes a concentraciones elevadas o con tiempos de contacto prolongados.
- El HDPE, ampliamente usado en farmacéutica y química, ofrece una resistencia química superior frente a la mayoría de los solventes, ácidos y bases, siendo el material de referencia cuando el agente desinfectante es agresivo.
- El PP, por su estructura química semicristalina, es resistente a ácidos y bases; y presenta buena resistencia térmica en aplicaciones industriales, lo que lo habilita para procesos donde el desinfectante se aplica con calor.
El riesgo concreto de no verificar compatibilidad es la migración de compuestos del polímero hacia el producto envasado, la deformación del envase o la reducción de su vida útil estructural.
Formación de biopelículas (biofilms)
Los biofilms representan uno de los problemas más subestimados en higienización industrial. Se trata de comunidades de microorganismos adheridas a superficies, embebidas en una matriz extracelular que actúa como barrera frente a los biocidas. Los microorganismos dentro de un biofilm establecido pueden presentar una resistencia significativamente mayor a los desinfectantes convencionales que sus equivalentes en estado planctónico.
En envases plásticos con geometría compleja, zonas de difícil acceso o superficies rugosas por desgaste, las condiciones para su formación son favorables: humedad constante, restos de materia orgánica y baja circulación de agente desinfectante. Además, las técnicas de verificación estándar (placas de contacto, bioluminiscencia) detectan la presencia de microorganismos pero no la matriz del biofilm en sí. Y esto puede dar resultados negativos falsos en superficies con colonización establecida.
Consumo energético y huella de carbono
El costo energético e hídrico de los procesos de desinfección en la industria alimentaria y farmacéutica no siempre está cuantificado. En este contexto, la selección de agentes desinfectantes que no requieran enjuague adicional, como es el caso de OXIBAC® – SILVER TP 20, tiene implicaciones directas sobre la huella operativa de una planta. Esto no es solo una cuestión ambiental: tiene impacto directo sobre la eficiencia operativa y los costos del proceso.
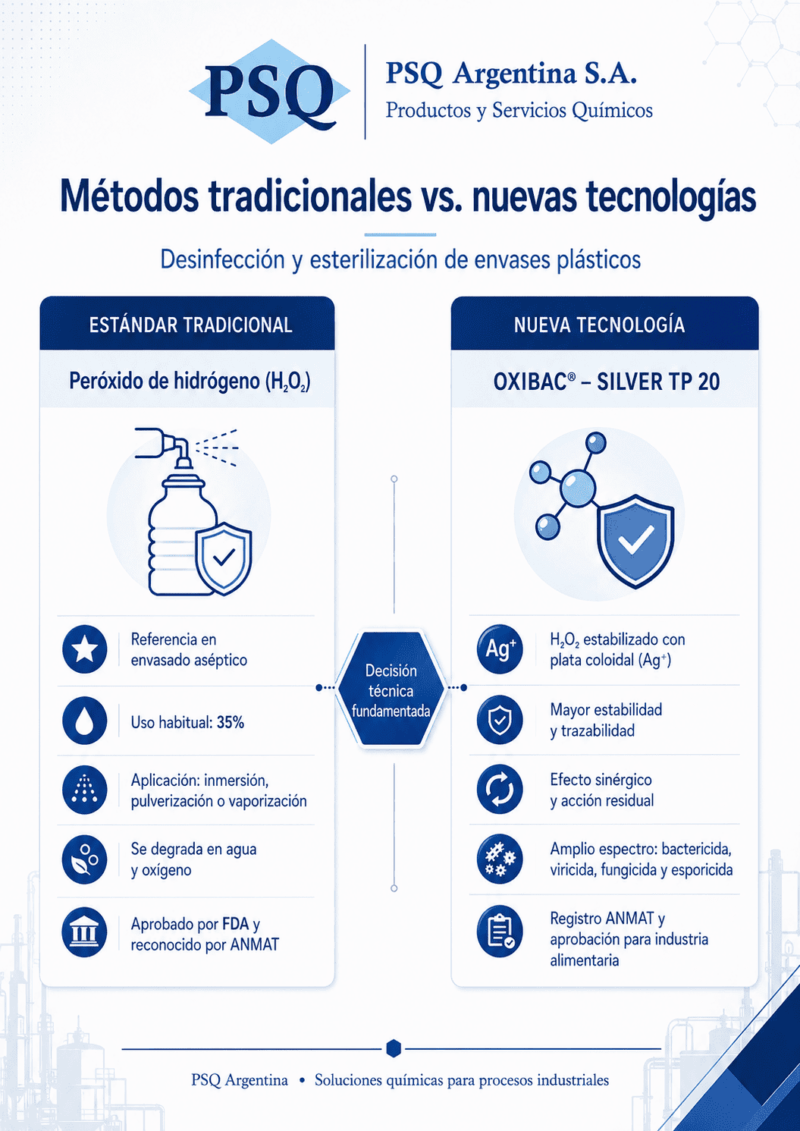
Métodos tradicionales vs. Nuevas tecnologías
Hay un estándar consolidado que domina la industria del envasado aséptico desde hace décadas. Sin embargo, existen formulaciones más recientes que amplían las opciones disponibles con ventajas operativas concretas. Entender qué ofrece cada alternativa es lo que permite tomar una decisión técnica fundamentada.
El estándar: peróxido de hidrógeno
El H₂O₂ es la sustancia de referencia en la desinfección y esterilización de envases plásticos. La mayoría de los sistemas de envasado asépticos lo utilizan a una concentración del 35%, más raramente al 25%, aplicado por inmersión en baño o por pulverización. Su uso está aprobado por la FDA para el tratamiento y limpieza de envases en contacto con alimentos (CFR, Título 21, Volumen 3), y en Argentina, la ANMAT lo reconoce como agente biocida apto para superficies inertes en la industria alimentaria.
Su mecanismo de acción se basa en la oxidación de componentes celulares críticos de los microorganismos, con una eficacia de amplio espectro. Una ventaja operativa relevante: al degradarse, genera únicamente agua y oxígeno, por lo que no requiere enjuague adicional con agua estéril, simplificando el proceso y reduciendo consumo hídrico. La tecnología de vaporización, en particular, asegura cobertura uniforme en superficies internas de geometría compleja.
La innovación en química estabilizada: OXIBAC® – SILVER TP 20
El peróxido de hidrógeno tiene limitaciones muy conocidas en la industria:
- Su potencia varía con el pH, la temperatura y la presencia de materia orgánica.
- Tiene un tiempo de vida útil en solución limitado.
Para resolver esas restricciones, desarrollamos OXIBAC® – SILVER TP 20, una formulación de peróxido de hidrógeno estabilizado con plata coloidal (Ag⁺) diseñada para entornos industriales donde la consistencia de la concentración activa y la trazabilidad del producto son parte del sistema de calidad.
La combinación no es arbitraria. Estudios técnicos documentan que la acción sinérgica del H₂O₂ y la plata potencia la actividad desinfectante de cada componente por separado, actuando mediante mecanismos redox cíclicos que generan daño celular acumulativo en el microorganismo.
A eso se suma un posible efecto residual de la plata sobre superficies, que puede contribuir a reducir la recolonización microbiológica entre ciclos de aplicación. El resultado es una formulación de amplio espectro (bactericida, viricida, fungicida y esporicida) que mantiene activos ambos componentes durante el tiempo de almacenamiento, resolviendo uno de los problemas históricos de estas combinaciones. Además, cuenta con registro vigente en ANMAT y aprobación para uso en la industria alimentaria en Argentina.
¿Cómo implementar un protocolo eficaz de sanitización?
Un protocolo de sanitización es una secuencia de decisiones técnicas donde cada etapa depende de la anterior. El orden de los pasos no es intercambiable, y omitir alguno invalida los siguientes.
1. Caracterización del sustrato.
Identificar el tipo de polímero del envase (PET, HDPE, PP u otro) y verificar la compatibilidad química con el agente desinfectante previsto. La compatibilidad debe validarse con datos del fabricante del plástico o con ensayos de inmersión bajo condiciones reales de proceso.
2. Evaluación de la carga microbiológica inicial
Antes de definir el nivel de tratamiento requerido (sanitización, desinfección o esterilización), es necesario conocer la carga biológica del envase en condiciones de uso normales. Esto determina la exigencia del protocolo y los parámetros de validación.
3. Pre-limpieza
Ningún agente biocida actúa eficazmente sobre superficies con carga orgánica residual. El paso de limpieza previo no es optativo: elimina sustratos que protegen a los microorganismos y comprometen la penetración del desinfectante. Esta secuencia está alineada con las Buenas Prácticas de Manufactura (BPM) y los sistemas APPCC aplicables.
4. Selección del agente y método de aplicación
Elegir entre inmersión en baño, pulverización o vaporización según la geometría del envase, el nivel de esterilidad requerido y las restricciones del proceso (temperatura, tiempo disponible, riesgo de residuos). Para líneas asépticas con requerimientos documentados, el H₂O₂ al 35% en sus variantes homologadas es el estándar técnico y regulatorio.
5. Validación y monitorización
El protocolo no es válido sin evidencia de eficacia. Los indicadores biológicos, los controles de ATP por bioluminiscencia y los registros de concentración activa del agente son herramientas básicas de validación. Para biofilms, se requieren técnicas complementarias que detecten la matriz extracelular, no solo la presencia de microorganismos viables.
6. Documentación y trazabilidad
En sectores regulados, la trazabilidad del proceso de desinfección es parte del sistema de calidad. Cada lote de producto desinfectante utilizado debe tener número de registro, concentración verificada y condiciones de aplicación registradas.
Cuando el envase es el último punto de contacto con el producto, cada decisión es importante: el agente elegido, el tiempo de contacto, la compatibilidad con el plástico y la forma en que se documenta el proceso.
En PSQ Argentina desarrollamos soluciones químicas pensadas para integrarse a protocolos exigentes de higiene industrial, con soporte técnico para adaptar cada aplicación a las condiciones reales de planta.
¿Necesitas definir o ajustar un protocolo de sanitización, desinfección o esterilización para envases plásticos? Contacta con nuestro equipo técnico y evaluemos juntos la solución más adecuada para tu proceso.